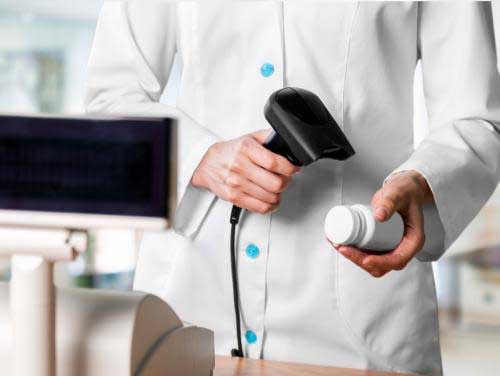
Средства идентификации будут использованы для первичной упаковки лекарственных препаратов (для медицинского применения) и для вторичной (потребительской). Важно уточнить, что оператором системы маркировки могут выступать только государственные организации, определяемые Правительством Российской Федерации.
В том числе, кабинет министров установит характеристики средства идентификации, порядок его нанесения, требования к формату и структуре маркировки, а также к мониторингу движения лекарственных препаратов.
Кроме того, в июле 2018 года планируется провести в Государственной Думе парламентские слушания по ходу реализации законодательной инициативы. На них будут даны рекомендации Правительству РФ по подготовке нормативно-правовых актов, вытекающих из данного законопроекта.
За производство и продажу немаркированных медикаментов законом предусмотрена ответственность. Напомним, что санкции установлены и за внесение ложной информации о препаратах в систему мониторинга движения лекарств.